Nový nástroj pro rozsáhlé úpravy genomu
16.12.2020 |
Odborníci z Kalifornské univerzity v San Francisku vyvinuli nový nástroj pro odstranění velkých úseků DNA z genomu buňky. Nový systém, nazvaný CRISPR-Cas3, byl představen v časopise Nature Methods.
Obrovská síla a význam sady nástrojů CRISPR-Cas byly letos podtrženy udělením Nobelovy ceny za chemii dvěma vědkyním, Jennifer Doudnaové a Emmanuelle Charpentierové, které ji vyvinuly a v roce 2012 poprvé použily.
Systémy CRISPR-Cas jsou rozmanitou skupinou nukleáz (enzymy štěpící DNA hydrolýzou fosfodiesterových vazeb nukleových kyselin) naváděných na místo štěpení pomocí RNA, které poskytují prokaryotním organismům schopnost obrany proti virovým částicím. Při setkání s fágem (virus napadající bakterie) mohou mikroby krátké úseky genetických prvků z virové DNA začlenit do svého vlastního genomu, do oblasti nazývané CRISPR. Při opakovaném napadení bakterie fágem se transkripcí CRISPR oblasti vytváří CRISPR RNA (crRNA), na které se vážou tzv. Cas nukleázy; crRNA, která je komplementární k fágové DNA, tak může nasměrovat připojené nukleázy na cizorodou DNA.
Systémy CRISPR-Cas se dělí do dvou tříd: systémy třídy 1 používají k degradaci cizích nukleových kyselin komplex proteinů Cas a systémy třídy 2 používají pro stejný účel jediný velký protein Cas.
Aplikace pro genové úpravy se zaměřují zejména na systémy CRISPR s jedinou podjednotkou třídy 2 (např. Cas9 a Cas12a). Široce používaný soubor CRISPR-Cas9 je často označován jako molekulární nůžky, které mohou rychle a přesně vyříznout malý kousek DNA v cílovém místě. Avšak nejčastěji používané enzymy Cas9 a Cas12a mají omezenou schopnost provádět velké delece.
Velký potenciál pro technologie genomových úprav mají i systémy třídy 1, přestože se skládají z komplexů s více podjednotkami. Vzorovým genem v systémech třídy 1 typu I je Cas3, „jednořetězcový“ 3′‑5 ′ enzym s DNA helikázovou-nukleázovou aktivitou, který na rozdíl od Cas9 nebo Cas12a účinně degraduje cílovou DNA. A právě systémy Cascade-Cas3 (Cascade = CRISPR-associated complex for antiviral defense) je možné po úpravě použít jako nástroje pro velké genomové delece.
Kalifornští vědci ve své studii použili a optimalizovali systém CRISPR typu I-C od Pseudomonas aeruginosa (PaeCas3c) pro endogenní i heterologní genomové inženýrství u čtyř mikrobiálních druhů. Ve srovnání s jinými systémy typu 1, jako je dobře studovaný systém typu I-E (šest různých proteinů), je typ I-C zjednodušený a vyžaduje pouze čtyři proteiny (cas3, cas5, cas8, cas7). Pro určení místa štěpení DNA byla k navádění použita jediná CRISPR RNA (crRNA) a Cas3 generoval z místa určeného naváděcí RNA delece oběma směry. V Pseudomonas aeruginosa se podařilo generovat velké delece (7–424 kb) s téměř 100% účinností, zatímco systém s Cas9 poskytoval malé delece a bodové mutace. Při opakovaném použití se podařilo zmenšit genom o více jak 800 kb (13,6 % genomu).
Cascade–Cas3 je tedy schopný provádět účinné delece na úrovni genomu, jichž v současné době nelze dosáhnout jinými metodami. Má potenciál sloužit jako výkonný nástroj pro základní výzkum, objevování a optimalizaci kmenů při cíleném odstraňování celých genů, genových klastrů, profágů nebo plazmidů, tedy úkolů, kde jsou systémy třídy 2 neúčinné. Hranice velkých delecí byly efektivně specifikovány HDR templátem během editace pomocí Cascade–Cas3. Přenosový vektor „vše v jednom“ byl dále testován a ukázal se jako funkční u bakterií Escherichia coli, Pseudomonas syringae a Klebsiella pneumoniae.
„Cas3 je jako Cas9 s motorem - po nalezení své specifické DNA sekvence „běží“ po DNA a žvýká ji jako Pac-Man,“ uvedl Joseph Bondy-Denomy, jeden z autorů studie.

CRISPR–Cas3 je zvláště slibný nástroj pro použití v eukaryotických buňkách, protože může usnadnit zkoumání velkých segmentů nekódující DNA, z nichž většina má zatím neznámou funkci. Nedávno bylo navíc prokázáno, že „genové knockouty“ generované Cas9 (tj. malé indely způsobující změny čtecího rámce) často kódují pseudo-messengerové RNA, které mohou produkovat proteinové produkty; to může vyžadovat použití metod pro úplné odstranění genu.
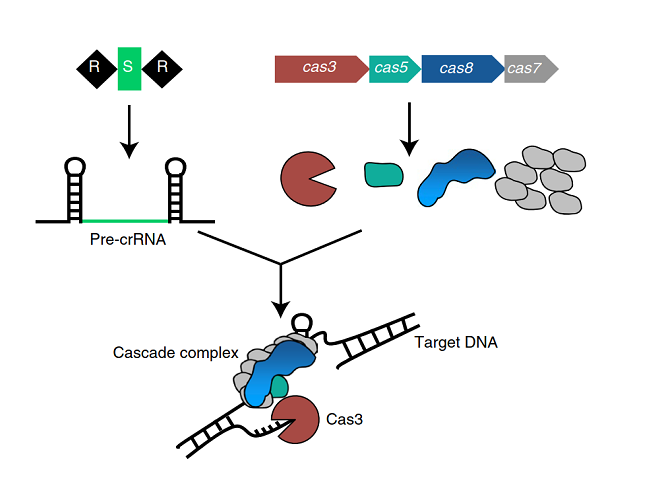
Obrázek: Schéma operonu genu cas typu I-C a CRISPR struktury. Systém je tvořen Cas proteiny (Cas51: Cas81: Cas77) a jednou crRNA, která navede Cas3 na rozpoznávánou cílovou DNA. Cas3 poté degraduje DNA svojí duální helikázovou-nukleázovou aktivitou.
Autoři poskytli použité plazmidové konstrukty včetně „all-in-one“ varianty společnosti Addgene (neziskové plazmidové úložiště), takže jsou dostupné za manipulační poplatek pro neziskové laboratoře po celém světě: https://www.addgene.org/133773/.
Zdroje:
Csörgő, B., León, L.M., Chau-Ly, I.J. et al. A compact Cascade–Cas3 system for targeted genome engineering. Nat Methods 17, 1183–1190 (2020).
https://doi.org/10.1038/s41592-020-00980-w
Více také v Nature Methods a Phys.org.